ЛАБОРАТОРНА РОБОТА № 3
ВИЗНАЧЕННЯ КРИТИЧНИХ ТОЧОК І ПОБУДОВА ДІАГРАМИ СТАНУ СПЛАВІВ ’’СВИНЕЦЬ - СУРМА’’
Мета роботи: освоїти методику побудови кривих охолодження металів і сплавів, визначення на них критичних точок методом термічного аналізу; навчитися будувати та аналізувати діаграми стану подвійної системи на прикладі сплаву свинець – сурма.
Матеріали та обладнання. Для виконання даної лабораторної роботи необхідні такі матеріали та обладнання: електрична піч, термопара, тиглі з навісками свинцю, сурми та їх сумішей, мілівольтметр зі шкалою від 0 до 500 мВ.
Теоретичні відомості.
При нагріванні відбувається плавлення твердих тіл, при охолодженні – їх кристалізація (crystallization) (затвердіння). Будь-які зміни в стані металу або сплаву (фазові, структурні перетворення) супроводжуються тепловим ефектом. При нагріванні відбувається поглинання тепла, а при охолодженні – виділення тепла.
Температури, при яких відбуваються зміни стану сплаву, називаються критичними. Реєстрація зміни температури сплаву в часі здійснюється термічним методом.
При термічному аналізі за експериментальними даними будують графіки залежності зміни температури сплаву в часі в процесі охолодження (або нагрівання) з постійною швидкістю. Такі графічні залежності називаються кривими охолодження або нагрівання.
При охолодженні аморфного тіла, наприклад смоли або скла, його температура буде спадати поступово і безперервно, перехід з рідкого стану в твердий буде поступовим. Графік нагрівання матиме вигляд кривої I, показаної на рис. 3.1, а. Крива охолодження II буде являти собою дзеркальне відображення кривої нагрівання.
Кристалічні речовини мають певну фіксовану температуру плавлення або кристалізації. Графік нагрівання чистого металу, побудований в осях координат час - температура, матиме вигляд кривої I, показаної на рис. 3.1, б. Графік охолодження чистого металу буде являти собою дзеркальне відображення графіка нагрівання (рис. 3.1, б, крива II).
Точка 1 на графіку охолодження відповідає початку кристалізації, точка 2 - закінченню кристалізації. На графіку нагрівання точка 1 відповідає початку плавлення, а точка 2 – закінченню плавлення. Процеси кристалізації і плавлення здійснюються при постійних температурах (на графіках – горизонтальна площадка, нижче якої метал знаходиться в твердому стані, вище – в рідкому).
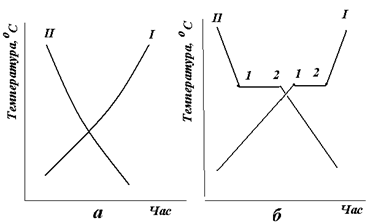
Рисунок 3.1 – Графіки нагрівання і охолодження:
а - аморфного тіла; б - кристалічного тіла (чистого металу).
Ці температури, а також температури будь-яких інших змін в стані металу або сплаву, які спостерігаються в ньому при нагріванні або охолодженні і супроводжуються поглинанням або виділенням тепла, як і відповідні їм точки на графіках нагрівання або охолодження, називаються критичними.
По критичних точках температурних кривих (наприклад, початок або кінець кристалізації) будують діаграму стану сплаву.
Діаграма стану сплавів (constitution diagram, equilibrium diagram) - це графічне зображення зміни структури і фазового складу сплавів в залежності від температури та концентрації.
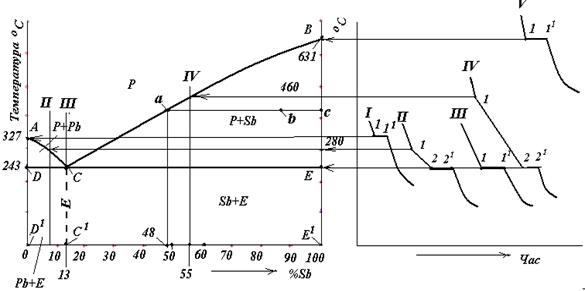
На рис. 3.2 зображена діаграма стану сплавів свинець – сурма в координатах температура (°С) - концентрація компонентів (%). Початок осі абсцис (вісь концентрацій) відповідає 100% свинцю і 0% сурми; кінець осі абсцис - 0% свинцю і 100 % сурми.
Лінію АСВ, по якій рідкий сплав при охолодженні починає кристалізуватись (твердіти), називають лінією ліквідусу (liquidus line) (ліквідус - рідина). Лінію DCE, по якій закінчується кристалізація сплаву, називають лінією солідус (solidus) (солідус - твердий).
Сплав з концентрацією компонентів: Sb = 13 %, Pb = 87 % називається евтектичним (від грецького - легкоплавкий). Евтектичними називаються сплави, для яких характерно:
1. Початок і кінець кристалізації відбуваються при одній і тій же температурі (точки ліквідус та солідус збігаються);
Рисунок 3.2 – Діаграма стану та криві охолодження сплавів свинець – сурма
2. Найменша температура плавлення серед сплавів даної системи;
3. Структура таких сплавів є механічною сумішшю компонентів ( в даному випадку свинцю та сурми).
Сплави, які мають концентрацію сурми менше, ніж евтектичний (менше 13%) і розміщені на діаграмі лівіше точки С називаються доевтектичними.
Сплави, що мають концентрацію сурми більше евтектичного і розміщені правіше точки С на діаграмі, називаються заевтектичними.
З діаграми видно, що доевтектичні сплави мають температури кристалізації (або плавлення) по лінії АС; заевтектичні - по лінії СВ. Кінець кристалізації всіх сплавів закінчується утворенням евтектики (лінія DCE).
Сплави різної концентрації мають різну структуру, а отже і різні властивості. Вище лінії АСB сплави будуть рідкими. На ділянці АСD буде рідкий сплав з кристалами свинцю, на ділянці СВЕ буде рідкий сплав з кристалами сурми. Нижче лінії DCE буде твердий сплав.
По лінії СС1 – евтектичний сплав, на ділянці DСС1D1 – сплав складається з кристалів евтектики і кристалів свинцю, це сплав доевтектичний. На ділянці СЕЕ1С1 - заевтектичний сплав, він складається з кристалів евтектики і кристалів сурми.
Діаграма стану сплаву свинець – сурма є діаграмою першого роду.
За діаграмою стану першого роду кристалізуються сплави, компоненти яких в рідкому стані необмежено розчиняються один в одному, а в твердому стані зовсім не розчиняються і утворюють механічну суміш компонентів. За діаграмою стану першого роду кристалізуються такі сплави як: олово – цинк, свинець – сурма та інші.
В процесі кристалізації змінюється і концентрація компонентів в фазах, і кількість кожної фази сплаву (при кристалізації кількість твердої фази збільшується, а рідкої зменшується).
Фазою (phase) називається хімічно однорідна частина сплаву, відокремлена від інших його частин поверхнею розділу (границею). Фазами в сплавах можуть бути хімічні елементи, хімічні сполуки, рідкі та тверді розчини.
В будь-якій точці діаграми, коли в сплаві одночасно існують дві фази, можна визначити кількість обох фаз і їх концентрацію. Для цього служить правило відрізків або правило важеля.
Правило відрізків (правило важеля) застосовують для визначення:
1. Концентрації компонентів в фазах;
2. Кількості (ваги) фаз сплаву в будь-якій точці діаграми.
Використаємо правило відрізків для аналізу стану сплаву в точці b (рис. 3.2). Проведемо горизонтальну лінію (коноду) через точку b до перетину з лініями діаграми. Одержимо лінію ас. Точка b ділить лінію ас на відрізки аb і bс.
Для визначення концентрації компонентів в фазах необхідно з точок перетину коноди з лініями діаграми опустити перпендикуляри на вісь концентрацій (вісь абсцис) діаграми стану (рис. 3.2).
Наприклад, в точці b (рис. 3.2) сплав складається з кристалів сурми і рідини. Опустивши перпендикуляр з точки а на вісь концентрацій, визначимо концентрацію компонентів в рідині. Вона становить 48 % Pb та 52 % Sb. Опустивши перпендикуляр з точки с на вісь абсцис, побачимо, що тверда фаза в даній точці складається з кристалів сурми (100 % Sb).
Відповідно до правила відрізків, кількість (вага), наприклад, твердої фази – кристалів сурми – в даній точці діаграми так відноситься до кількості всього сплаву, як довжина відрізка, що прилягає до лінії ліквідус аb, відноситься до повної довжини лінії ас.
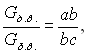 звідки:
звідки: 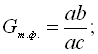
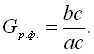
На рис. 3.2 зображені криві охолодження для чистих металів (Pb, Sb) I, V та їх сплавів II, III, IV.
Для аналізу кривих охолодження застосовують правило фаз (закон Гіббса), яке виражається формулою
С = К- Ф + 1,
де: С - число ступенів вільності, тобто число зовнішніх факторів (температура, концентрація), які можна змінювати без зміни числа фаз в сплаві; К - число компонентів ( в сплавах свинець - сурма К = 2, це свинець і сурма); Ф - число фаз.
Температура плавлення чистого свинцю - 327 °С, сурми - 630 °С.
Доевтектичному сплаву (6 % Sb, 94 % Pb) відповідає крива II. Вище точки 1 сплав знаходиться в рідкому стані і має одну фазу, тоді С = 2-1+1=2. При двох ступенях вільності в цій області можна змінювати концентрацію та температуру, а сплав залишиться однорідним – рідким. Крива охолодження круто спадає вниз.
Точка 1 - початок кристалізації, точка 2 - закінчення кристалізації. В інтервалі температур від точки 1 до точки 2 проходить утворення кристалів свинцю, на цій ділянці сплав являє собою суміш рідини і кристалів свинцю. Тобто між точками 1 і 2 існує дві фази - рідка і тверда: С = 2-2+1=1. При одному ступені вільності незалежною змінною є тільки температура. Із зменшенням температури сплаву кристалів утворюється більше, рідини залишається менше.
На ділянці 2-2? залишки рідини кристалізуються в механічну суміш свинцю та сурми – евтектику, де матимемо три фази (кристали свинцю, кристали сурми і рідкий сплав). Число ступенів вільності С = 2-3+1=0. При цьому виділяється велика кількість теплоти і температура залишається постійною.
Нижче точки 2 сплав знаходиться повністю в твердому стані і його структура складається з кристалів свинцю та евтектики (дрібнодисперсної суміші кристалів свинцю та сурми). Таким чином, сплав в даній області складається з двох фаз - кристалів свинцю і сурми: С=2-2+1=1.
Крива III – охолодження евтектичного сплаву ( 13 % Sb, 87 %Pb). Евтектичний сплав має криву охолодження аналогічну кривій чистого металу, тільки із більш швидким охолодженням розчину. Кристалізація протікає при сталій температурі і концентрації (в точці С). Утворюється механічна суміш компонентів (свинцю та сурми).
Заевтектичному сплаву відповідає крива IV. Точка 1 відповідає початку кристалізації, 2 - кінцю кристалізації. В інтервалі температур від 1 до 2 проходить утворення кристалів сурми. На цій ділянці сплав являє собою суміш рідини та кристалів сурми. Із зниженням температури сплаву кристалів утворюється більше, рідини залишається менше. На ділянці 2-2? залишок рідини кристалізується в механічну суміш кристалів свинцю та сурми (евтектику) (eutectic).
Схеми мікроструктури сплавів після охолодження показані на рис. 3.3.
Схеми мікроструктури: а – чистий свинець, б - доевтектичний сплав, в – евтектичний слав, г - заевтектичний сплав.
Аналіз мікроструктури показує, що залежно від концентрації компонентів змінюється мікроструктура сплаву.
Діаграма стану дає можливість визначити стан сплаву при будь-якій температурі та заданій концентрації.
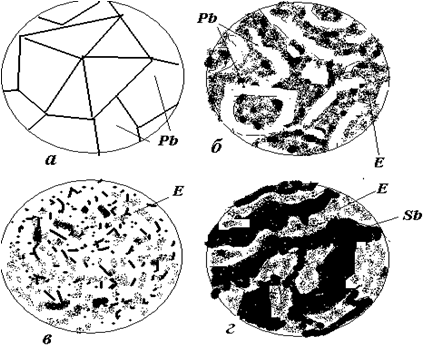
Рисунок 3.3 – Структура сплавів свинець – сурма:
а – чистий свинець; б – доевтектичний сплав;
в – евтектичний сплав; г – заевтектичний сплав
Установка для термічного аналізу
Установка для термічного аналізу (рис. 3.4) складається з нагрівальної та контролювальної апаратури.
Навіски 3 в тиглях з заданою концентрацією компонентів (Pb, Sb) доводять до повного розплавлення з перегрівом на 20...30 °С в муфелі електропечі 1. Контроль температури здійснюється хромель-алюмелевою (ХА) термопарою 4, підключеною до потенціометра 5. Після того, як температура буде достатньою для термічного аналізу, тигель з навіскою установлюють на вогнетривку підставку. Холодні кінці термопари з'єднані з клемами вимірювального приладу 5 - мілівольтметра ВЗ-36. Для знаходження відповідності показань мілівольтметра (мВ) значенням температури сплаву (°С) проводять тарування термопари. Дані заносяться в таблицю .
Слід відзначити, що отриманими даними (табл. 3.1) можна користуватися тільки для даної термопари. Це і є таруванням термопари. Отримані дані мілівольтметра (мВ) під час досліду згідно з таблицею переводять в відповідні значення температур (°С).
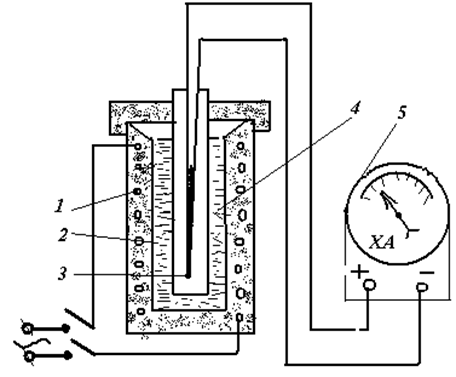
Рисунок 3.4 – Схема установки для визначення критичних точок металів і сплавів:
1 – електропіч; 2 – тигель; 3 – термопара;
4 – розплавлений метал (сплав); 5 – гальванометр.
Порядок виконання роботи
1. Тиглі з чистими свинцем, сурмою та трьома сплавами: доевтектичним (6% сурми), евтектичним (13% сурми) та заевтектичним (55% сурми) нагрівати в електричній печі. Температуру заміряти гальванометром термопари.
2. Виймати і охолоджувати тиглі потрібно в такій послідовності: евтектичний сплав – при досягненні температури 260…270 оС, доевтектичний сплав – 290…300 оС, чистй свинець – 340…350 оС, заевтектичний сплав – 475…480 оС, чиста сурма – 645…650 оС фіксуючи показання гальванометра через 10…15 с до закінчення тверднення металу (сплаву). Результати замірів внести в таблицю.
Таблиця 3.1 – Результати замірів
τ, с |
||||||
V, мВ |
||||||
T, oС |
3. За результатами дослідів побудувати на міліметровому папері криві охолодження кожного металу (сплаву). При цьому зручно брати масштаб 10 с = 1 мм і 10о = 1 мм.
4. За кривими охолодження побудувати діаграму стану сплавів свинець – сурма, переносячи критичні точки з кривих охолодження на діаграму стану.
Зміст звіту
В звіті необхідно вказати:
Контрольні питання для самопідготовки
1. Що являє собою діаграма стану сплавів?
2. Які методи застосовують для побудови діаграм стану сплавів?
3. Які точки на кривих нагрівання чи охолодження називають критичними?
4. Поясніть значення термінів: евтектика, солідус, ліквідус.
5. Покажіть на діаграмі стану сплавів ці лінії та точки.
6. Чим пояснюється зміна швидкості охолодження сплаву?
7. Який з досліджених сплавів є евтектичним? доевтектичним? заевтектичним?