




27.5. Критичні теплові потоки і коефіцієнти тепловіддачі при кипінні розчинів, які не утворюють азеотропні суміші
На рис.27.15. наведені криві зміни критичних теплових потоків qкр1 від складу (концентрації компоненту Сўнк, який кипить при більш низькій температурі) для деякої
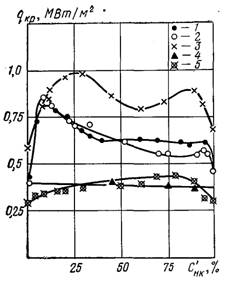
Рис.27.15. Залежність qкр1 від складу при об’ємному кипінні бінарної суміші органічних рідин у великому об’ємі: дифеніл – бензол, р = 0,2 МПа; 2 – МІПД – бензол, р = 0,2 МПа; 3 – дифеніл – бензол, р = 0,7, 8,5 МПа; 4 – суміш пари і метатерфенілів, р = 0,2 МПа; 5 – ацетон – толуол, 0,1 МПа
двокомпонентної суміші органічних рідин при об’ємному кипінні на зануреній поверхні. Як видно з рисунка, в одних випадках зміна складу суміші майже не впливає на значення qкр1, в інших критичні теплові потоки для суміші завжди вищі qкр1 чистих компонентів. Така залежність qкр1 від концентрації Сўнк не може пояснюватися зміною фізичних властивостей середовища.
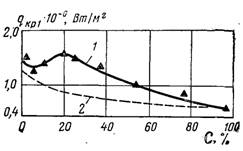
Рис.27.16. Залежність qкр1 від масової концентрації етанолу у воді: 1 – дослідні дані; 2 – розрахункова крива
На рис.27.16 дослідні значення критичних теплових потоків qкр1 для розчинів етанолу у воді співставленні з кривою, розрахованій теоретично при використанні фізичних властивостей суміші. У відповідності із зміною фізичних властивостей середовища qкр1 повинен безперервно зменшуватися від значень, отриманих при кипінні чистої води, до значень характерних для етанолу. Між тим дослідні значення qкр1 при низьких концентраціях спирту Сўнк вищі, ніж для чистої води, а при високих Сўнк хоч і нижчі, ніж для води, але перевищують розрахункові величини.
Для всієї розглянутої на рис.27.15 і 27.16 суміші (за винятком суміші пара – метатерфенол) чітко проявляється максимум на кривих qкр1 = f(Сўнк); іноді є два максимуму (крива 3 на рис.27.15)
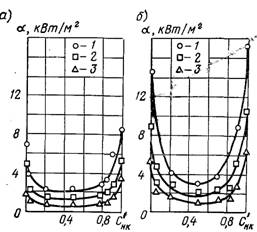
Рис.27. 17. Залежність коефіцієнта тепловіддачі від концентрації при кипінні дифеніл бензольної суміші на горизонтальній трубі діаметром 5 мм: а) – р = 0,108 МПа; б) – р = 0,8 МПа; при q кВт/м2: 1 – 200; 2 – 100; 3 – 50 [на рисунку допущена помилка, необхідно читати a, кВт/(м2·°С)]
Аналіз дослідних даних показує, що великий вплив на хід кривої qкр1 = f(Сўнк) оказує співвідношення в значеннях температур насичення компонентів, з яких складається суміш. Суміш низько киплячої рідини з високо киплячою максимальні величини qкр1 значно перевищують qкр1 для окремих компонентів. У той же час коефіцієнти тепловіддачі за цих умов значно менші a для чистих рідин (рис.27.17).
Отримані залежності qкр1 = f(Сўнк) і a = f(Сўнк) можна пояснити наступним чином. При кипінні бінарних розчинів високо киплячої (ВК) і низько киплячої (НК) рідин, які не утворюють азеотропної суміші, всередину парової бульбашки випаровується переважно НК компонент. Тому у межах киплячого пограничного шару концентрація ВК компоненту збільшується по відношенню до основної маси суміші, тобто у пограничному шарі поряд з градієнтом температур має місце градієнт концентрацій компонент. Тому що температура суміші залежить від її складу, то температура насичення рідини у прилеглому до поверхні шару оказується завжди вищою, ніж на відстані від неї. Рідина, яка підтікає до поверхні, нагрівається тут до температури, що перевищує температуру, яка повинна була б бути, якби концентрація у плівці була б такою ж, як і в основній масі суміші. На це тратиться додаткова кількість теплоти Dq. Збільшення кількості теплоти, яка передається одному і тому ж об’єму рідини, призводить до збільшення теплової енергії, яка виноситься молями паро рідинної суміші (внаслідок збільшення різниці між ентальпією рідини у пограничному шарі і на відстані від нього). Цей ефект тим більший, чим більша різниця температур між рідиною безпосередньо біля поверхні теплообміну і в основній масі. Остання суттєво залежить як від різниці рівноважних концентрацій НК компонента в паровій СІнк і рідкій Сўнк фазах (DС = DСІнк – – DСўнк), так і від крутизни кривої насичення [кривої tн = f(Сўнк)]. Чим вище DС, тим при тій же інтенсивності процесу масообміну установиться більший градієнт концентрацій у пограничному шарі. У той же час одне і те ж значення DС окаже тим більший вплив на кількість теплоти, яка переноситься молями суміші, чим більша крутизна лінії насичення, тобто чим більший вплив концентрації на tн.
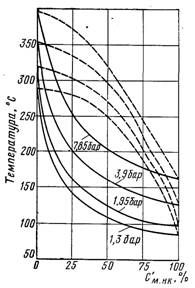
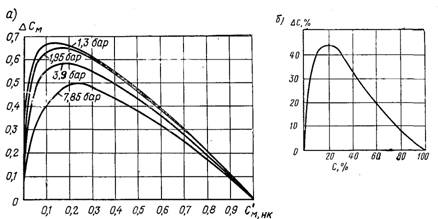
Рис.27.18. Криві насичення для суміші МІПД – бензол (Сўм.нк – молярна концентрація НК компонента в рідині): –––––––– – крива кипіння рідини; – – – – – крива сухої насиченої пари Рис.27.19. Залежність DС від Сўнк для бінарної суміші: а) – МІПД – бензол (молярні концентрації); б) – вода-етанол (масові концентрації)
На рис.27.18 наведені криві насичення (діаграма рівноваги) для суміші моноізопропілдифенілу (МІПД) з бензолом, на рис.27.19 залежності різниці концентрацій НК компоненту в паровій і рідкій фазах DС від Сўнк для тієї ж суміші. Криві насичення і залежності DС = f(Сўнк) для іншої розглядуваної суміші ВК і НК рідин мають аналогічний характер.
З рисунків видно, що DС спочатку зростає, а далі, при досягненні деякого найбільшого значення, починає зменшуватися. Крутизна кривої насичення для рідкої фази безперервно падає. Тому на початку, коли DС зростає, а tн зменшується при збільшенні концентрації НК компоненту, критичний тепловий потік збільшується. При цьому чим швидше зростає DС і крутіша крива tн= f(Сўнк) для рідкої фази, тим різкіше збільшується qкр1. У подальшому, коли DС і крутизна кривої насичення зменшуються, qкр1 падає (наявність різниці температур насичення у прилеглій до стінки плівці і масі суміші продовжує чинити позитивний вплив на кількість винесеної теплоти, але цей вплив менший, ніж при більш низьких концентраціях НК компоненту).
У залежності від форми кривої tн= f(Сўнк) і DС = f(Сўнк), а також теплофізичних властивостей рідин залежність qкр1 = f(Сўнк) може мати один чи два максимуми.
При великих концентраціях НК компоненту спочатку із збільшенням Сўнк у суміші (зміщуючись справа наліво по кривій насичення, рис.27.18) ВК компонент усе в більшій кількості збирається біля поверхні тепловіддачі. Ентальпія молів, які відриваються від поверхні, при цьому зростає. Зростає також ентальпія молів, які рухаються до поверхні, але спочатку основну дію чинить перший фактор, а у подальшому в залежності від форми кривої tн= f(Сўнк) для кожної фази у цій її частині збільшення температури насичення суміші може чинити переважний вплив, і тоді qкр1 після деякого збільшення починає падати. Другий максимум (якщо він має місце в правій частині графіка) завжди повинен бути меншим за перший, тому що в області низьких концентрацій НК компоненту збільшення DС супроводжується зменшенням tн, у той час як при високих значеннях Сўнк температура суміші при збільшенні Сўнк, навпаки, збільшується.
Для підвищених тисків зміна Dtн у залежності від Сўнк при низьких концентраціях НК компоненту відбувається менш стрімко, а невеликі значення DС досягаються при більш високих вмістах НК компоненту в суміші (див. рис.27.18 і 27.19). З цієї причини точка, яка визначає найбільше значення qкр1, зміщується в бік більш високих концентрацій Снк.
З поданого матеріалу стає зрозумілим, чому, наприклад, для суміші дифеніл – бензол чи МІПД – бензол максимальні значення перевищують критичні теплові потоки для чистих компонентів, у той час як для суміші паратерфенілу і метатерфенілу зміна qкр1 у залежності від складу суміші протікає практично по лінійній залежності (від більшого значення qкр1 для паратерфенілу до меншого – для метерфенілу, див рис.27.15). У суміші високо киплячого органічного теплоносія з бензолом температури насичення tн для чистих рідин відрізняються майже на 200°С, у той час як температура насичення паратерфенілу перевищує значення tн для метатерфенілу тільки на ~10°С. У перших двох сумішах безумовно найбільші значення різниці концентрацій НК компоненту DС у паровій і рідкій фазі також значно вищі, ніж у сумішах терфенілів.
Спостереження за механізмом процесу кипіння показали, що з ростом DС відривний діаметр бульбашки, середня швидкість їх росту і кількість діючих центрів пароутворення зменшується. Таким чином, хід кривих на рис.27.15 знаходить просте і логічне пояснення.
З наведених даних слідує, що для бінарної і багатокомпонентної суміші органічних рідин, близьких за своїми властивостями до ідеальних розчинів, практично теплові потоки змінюються по залежностям, які практично не мають екстремальних значень, якщо температури tн для окремих складових суміші близькі одна до одної; і, навпаки, при певних складах суміші qкр1 приймає значення qкр1,макс, який значно перевищує критичні теплові потоки для чистих компонентів, якщо tн для чистих речовин суттєво відрізняються між собою. Дані отримані на трійних сумішах високотемпературних теплоносіїв добре погоджуються з цим висновком.
Аналогічні міркування дозволяють вияснити, чому за цих умов коефіцієнти тепловіддачі зменшуються (рис.27.17). Якщо добавити до чистої ВК рідину з НК компонентом, температура суміші зменшиться значніше, ніж температура кипіння прилеглого до поверхні теплообміну шару, тому що концентрація ВК компоненту у шарі більша, ніж у масі рідини. Тому при тій же інтенсивності обміну числові значення a зменшуються (температурний перепад Dt зростає).
При додаванні у чисту НК рідину ВК компоненту, концентрація його збільшиться у плівці, яка прилягає до поверхні, у зв'язку з цим при тому ж тепловому потоці температура стінки підвищується. Це також призводить до збільшення Dt і зменшення коефіцієнта тепловіддачі a. Таким чином, у суміші органічних рідин, які відрізняються за значенням tн, критичний тепловий потік збільшується, а коефіцієнт тепловіддачі падає.
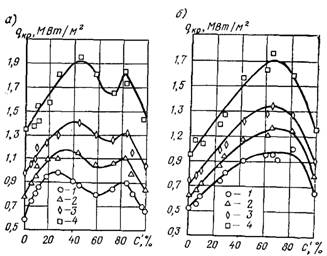
Рис.27.20. Значення qкр1 для суміші дифеніл бензолу: а) – р = 0,785 МПа; б) – р = 1,77 МПа; при Dtн,°С: 1 – 0; 2 – 25; 3 – 50; 4 – 100
На рис.27.20 наведені значення критичних теплових потоків для суміші дифеніл бензолу при поверхневому кипінні і різних значеннях Dtн. Тут же показані криві, отримані у тих же умовах при об’ємному кипінні (t = tн). Як видно з рисунка, при постійних значеннях Dtн (Dtн = tн – t) характер залежності qкр1 від складу в основному зберігається таким самим, як і при Dtн = 0, а вплив недогріву не відрізняється від впливу Dtн на qкр1 для чистих рідин (рис.27.21). Однак і за цих умов кількісні залежності, які установлені для однокомпонентних середовищ, не відображають специфіки процесу віддачі
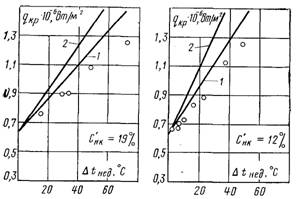
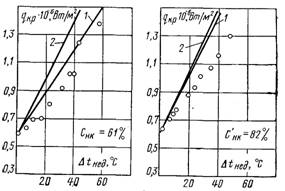
Рис.27.21. Вплив Dtн на qкр1 (суміш дифеніл бензолу, р = 0,118 МПа):1 – розрахункове значення; 2 – дослідні дані
теплоти до суміші і можуть використовуватися тільки для наближених розрахунків.
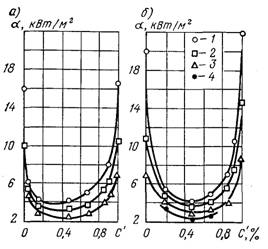
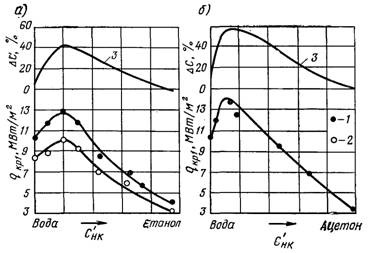
Рис.27.22. Значення коефіцієнта тепловіддачі при різних значеннях Dtн для суміші дифеніл бензолу при q = 290 кВт/м2 (кипіння на горизонтальній трубі діаметром 5 мм): а) – р = 0,353 МПа; б) – р = 0,8 МПа; при Dtн,°С: 1 – 0; 2 – 10; 3 – 30; 4 – 80; [на цьому рисунку допущена помилка, необхідно читати a, кВт/(м2·К)]
Рис.27.23. Критичні теплові потоки при поверхневому кипінні суміші в трубах (р = 0,66 МПа; Dtн = 50°С): а) – етанол-вода; б) – ацетон вода: 1 – w0 =5 м/с; 2 – w0 = 3,5 м/с; 3 – DС = f(Сўнк)
Як і для однокомпонентних рідин, при поверхневому кипінні суміші ступінь недогріву суттєво впливає інтенсивність тепловіддачі. Із збільшенням Dtн коефіцієнти тепловіддачі, які розраховані по температурному перепаду між стінкою і рідиною, падають (рис.27.22). Вплив концентрації суміші при поверхневому кипінні якісно залишається таким самим, як і за умови, коли температура рідини дорівнює tн.
Залежності qкр1 від складу при кипінні бінарної суміші трубах наведені на рис. 27.23. На рисунку наведені також криві, які установлюють зміну різниці концентрацій НК компоненту в парі і рідині в залежності від Сўнк. З рис.27.23 видно,
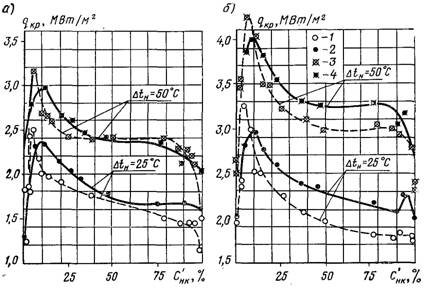
Рис.27.24.Критичні теплові потоки при поверхневому кипінні суміші МІПД-бензол у трубах і кільцевих каналах: а) – w0 = 4 м/с; б) – w0 = 8 м/с; 1, 3 – кільцевий канал, р = 0,294 МПа; 2, 4 – труба, діаметр 10 мм, р = 0,2 МПа
що характер впливу складу суміші на qкр1
залишається таким самим, як і при кипінні у великому об’ємі. Максимальні
значення критичних теплових потоків у цьому випадку також установлюються при DС близьких до DСмакс. Із збільшенням швидкості (так само як і для чистих рідин) значення критичних теплових потоків збільшуються. Аналогічні залежності qкр1 від Сўнк і w0 установлюються також при кипінні в кільцевих каналах (рис.27.24).
27.6. Теплообмін при кипінні розчинів, які утворюють азеотропні суміші
Як відомо, в азеотропних системах при певній концентрації складових Сўнк і Сўвк склад пари і рідини рівні і суміш веде себе як однокомпонентна рідина. Дослідження показали, що залежності qкр = f(Сў) і a = f(Сў) в розчинах, які утворюють азеотропні суміші носять ще більш складний характер.
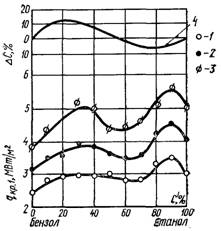
Рис.27.25. Критичні теплові потоки при поверхневому кипінні азеотропної суміші бензол-етанол (w0 = 5 м/с) при Dtн °С: 1 – 30; 2 – 50; 3 – 70; 4 – DС = f(Сў)
На рис.27.25 наведені криві зміни критичних теплових потоків при поверхневому кипінні суміші бензол – етанол. Ця суміш у азеотропній точці має склад: 32,4% бензолу і 67,6% етанолу. На рисунку показана також крива, яка визначає значення DС у залежності від складу суміші.
Як видно з цих залежностей, максимальні значення qкр1 знаходиться біля екстремальних точок на кривій DС = f(Сўнк), а мінімальні – в азеотропній точці чи біля неї. Це дає підставу розглядати таку суміш як суміш одного з компонентів з розчином азеотропного складу, а систему з азеотропною точкою у цілому – як дві окремі суміші. Якщо такий підхід є правильним, то криві зміни коефіцієнта тепловіддачі у залежності від складу (у відповідності з розглянутим вище механізмом тепло і масообміну в бінарних сумішах) повинні мати два мінімуми, а найбільші значення a для суміші повинні знаходитися в азеотропній точці.
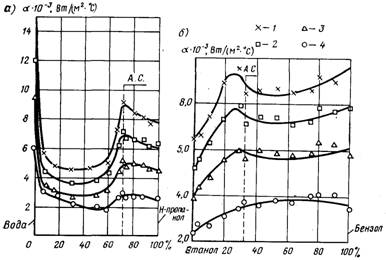
Рис.27.26. Коефіцієнт тепловіддачі при кипінні азеотропної суміші у великому об’ємі а) – вода-пропінол; б) – етанол-бензол при q, кВт/м2: 1 – 232; 2 – 175; 3 – 116; 4 – 58
При кипінні азеотропної суміші вода-пропанол (рис.27.26,а) така картина спостерігається досить точно. У той же час, в інших випадках (рис.27.26,б) має місце помітне відхилення отриманих залежностей від очікуваних при урахуванні тільки розглянутих вище впливів. Це, ймовірно, пов’язано з тим, що в реальних умовах поряд з основною причиною, яка обумовлює той чи інший характер протікання процесів, великий вплив може оказувати ряд інших факторів (хід кривих зміни концентрації складових суміші у плівці, яка прилягає до поверхні нагріву, теплофізичні властивості рідин і їх суміші та ін.).
При кипінні розчинів нелетких речовин у парову фазу переходить майже виключно розчинник. Тому навколо парової бульбашки і особливо в шарі, який прилягає до поверхні теплообміну, концентрація розчиненої речовини оказується більшою, ніж у масі розчину. Температура насичення розчину біля поверхні при цьому збільшується і навіть при одній і тій же інтенсивності процесу масообміну, якщо тепловий потік залишається постійним, температура стінки повинна бути вищою, ніж при кипінні однорідної рідини. Із збільшенням концентрації розчиненої речовини Ср цей ефект (до певних значень Ср) повинен підсилюватися. Таким чином, із збільшенням Ср коефіцієнт тепловіддачі, розрахований за температурним перепадом між стінкою і масою киплячої рідини, повинен зменшуватися. Однак така залежність a = f(Ср) не може бути безмежною. При певній концентрації розчину вміст розчиненої речовини у шарі, який безпосередньо прилягає до поверхні теплообміну, досягає насичення і з подальшим підвищенням Ср не змінюється, а між тим температура кипіння розчину при цьому буде збільшуватися.
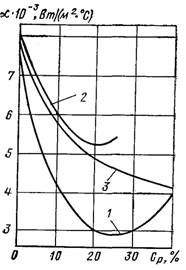
Рис.27.27. Залежність коефіцієнта тепловіддачі від концентрації Ср для розчинів нелетких речовин: 1 – водний розчин NaOH, q = 100 кВт/м2; 2 – водний розчин NaCl, q = 100 кВт/м2; 3 – водний розчин сечовини, q = 62,5 кВт/м2; 1 і 2 –кипіння у великому об’ємі; 3 – кипіння в трубах при w0 = 0,89 м/с
Усе це приводить до того, що температурний перепад між стінкою і рідиною починає зменшуватися, а a – збільшуватися. Таким чином, крива a = f(Ср) для розчинів нелетких речовин повинна проходити через мінімум. Існуючі дослідні дані повністю погоджуються з наведеними уявленнями про вплив Ср на інтенсивність теплообміну до розчинів, які складаються з нелетких речовин, про що свідчить рис.27.27.