4.4 СУЛЬФУРВМІСНІ СПОЛУКИ Серед великої кількості сульфурмісних сполук розглянемо тіоспир-ти ( ) та тіоетери ( ), які є тіоаналогами кисневмісних спо-лук, відповідно, спиртів та етерів. Наявність у атомів Сульфуру 3d-атомних орбіталей, на відміну від атомів Оксигену, обумовлює наявність інших сульфурвмісних сполук з більш високими ступенями окиснення Су-льфуру: сульфоксидів ( ) та сульфонів ( ). 4.4.1 Тіоспирти (тіоли, меркаптани) Тіоли – похідні сірководню, у молекулі якого атом Ггідрогену замі-щений на вуглеводневий радикал. Класифікація. Номенклатура. Загальна формула R–SH. В залежності від природи та будови ради-калу R сірковмісні сполуки поділяються на, відповідно, аліфатичні та аро-матичні тіоспирти та тіофеноли: 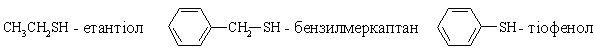 Назва за систематичною номенклатурою: базовий вуглеводень + су-фікс -тіол. Якщо SH-група не є головною, то при назві сполуки застосову-ють префікс меркапто-:  За винятком газоподібного метилмеркаптану, інші тіоли – рідини або тверді речовини. Їх температури кипіння вищі ніж у відповідних оксигенпохідних (табл. 4.18). Це пояснюється тим, що атоми Сульфуру, завдяки меншій електронегативності та більшому радіусу, порівняно з атомом Оксигену, не схильні до утворення водневих зв’язків. І, як наслідок, тіоли є менш розчинними у воді, ніж спирти та феноли. Меркаптани токсичні речовини із надзвичайно неприємним запахом, який помітний навіть у незначних кількостях. Наприклад, межова концентрація для виявлення етилмеркаптану за запахом складає 4,6•10-8 мг/л. Хімічні властивості тіоспиртів. Тіолати (меркаптиди) утворюються при взаємодії лужних металів або лугів із тіолами:  |