4.5.3 Будова карбонільної групи 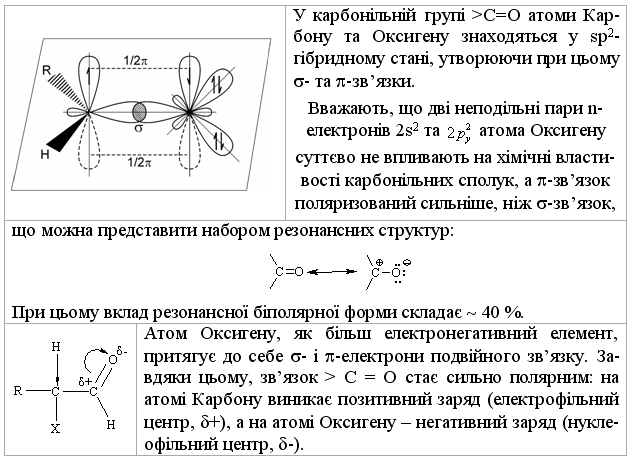 Альдегіди більш реакційноздатні сполуки, ніж кетони. Тому як, по-перше, наявність у кетонах ще однієї алкільної групи за рахунок +І-ефекту зменшує позитивний заряд на атомі Карбону карбонільної групи, а по-друге, при цьому виникають додатково стеричні фактори. Сильно поляризована карбонільна група (carbonyl group) впливає також і на рухливість атомів Гідрогену, що знаходяться в -положенні від-носно групи >C=O; у разі зменшення електронної густини на -атомі Карбону (Х – донор електронів) маємо зворотній ефект. Враховуючи впив індукційного ефекту, а також стеричні фактори, за реакційною здатністю карбонільні сполуки можна розташувати в ряд: 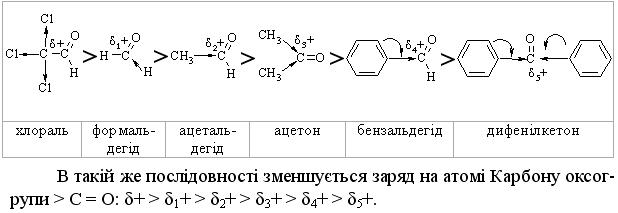 Хлораль і формальдегід здатні приєднувати навіть такий слабкий ну-клеофіл, як воду, а дифенілкетон не взаємодіє з таким полярним реагентом, як гідросульфіт натрію. Можна констатувати, що практично всі хімічні реакції альдегідів та кетонів обумовлені розподілом електронної густини в молекулі і найбільш характерними для них є: – реакції нуклеофільного приєднання (AN); – реакції за участю атома гідрогену, що знаходиться в -положенні відносно карбонільної групи; – реакції заміщення карбонільного Оксигену; – реакції окиснення та відновлення; – реакції полімеризації. Фізичні властивості альдегідів та кетонів. Альдегіди та кетони, на відміну від спиртів, не утворюють міжмоле-кулярних водневих зв’язків, тому їх температури кипіння значно нижче, ніж у спиртів. Деякі фізичні константи альдегідів та кетонів наведені, від-повідно, у табл. 4.22 та 4.23. Найпростіші альдегіди та кетони (ацетон, фо-рмальдегід, ацетальдегід) – розчинні у воді, а вищі добре розчинні у біль-шості органічних розчинників (спирти, етери, естери тощо). Альдегіди С1 – С4 мають різкий та неприємний запах, вищі – запах квітів (використову-ються у парфюмерії). |